Ecuador
Estos son los 4 lineamientos para la importación y venta de pruebas rápidas de autodetección de covid-19: ¿Cuándo inicia la medida?
La Agencia Nacional de Regulación, Control y Vigilancia Sanitaria (Arcsa) emitió los lineamientos para la importación y comercialización de pruebas rápidas de autodetección de covid-19 en el Ecuador, medida que entrará en vigencia el lunes 15 de agosto de 2022. En un comunicado difundido en Twitter la noche de este jueves 11 de agosto, Arcsa […]
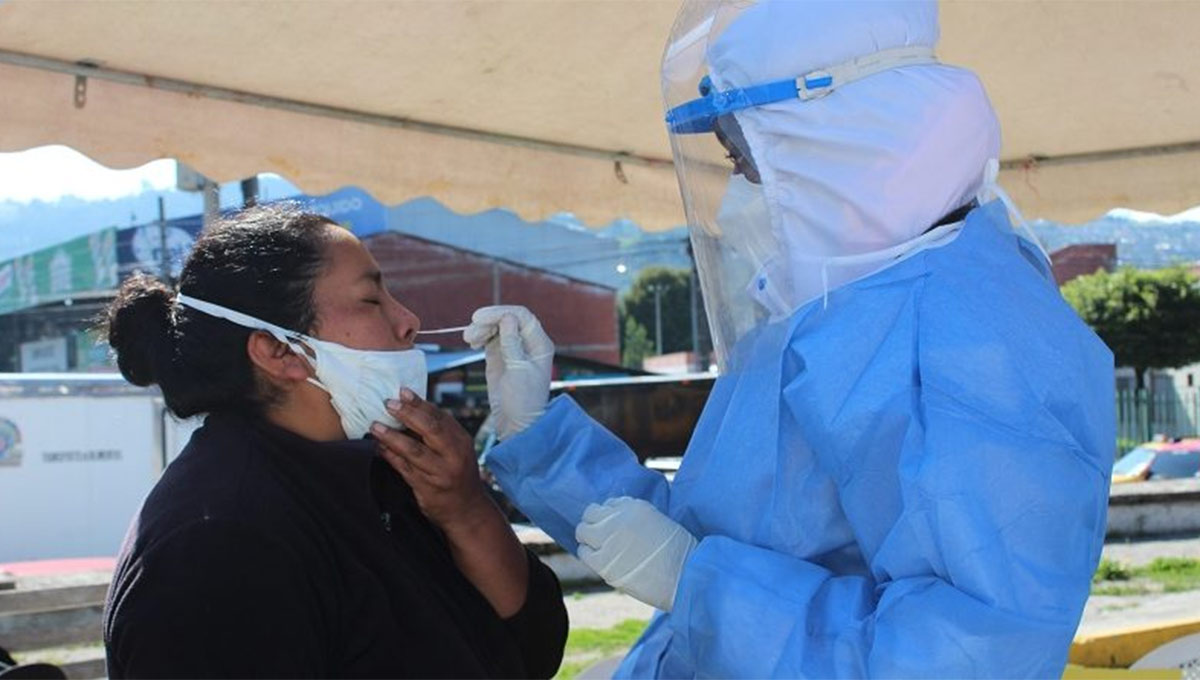
La Agencia Nacional de Regulación, Control y Vigilancia Sanitaria (Arcsa) emitió los lineamientos para la importación y comercialización de pruebas rápidas de autodetección de covid-19 en el Ecuador, medida que entrará en vigencia el lunes 15 de agosto de 2022.
En un comunicado difundido en Twitter la noche de este jueves 11 de agosto, Arcsa informa que tras la autorización por parte del Ministerio de Salud Pública (MSP) de la libre comercialización de pruebas rápidas de autodetección de covid-19, presenta los criterios para la importación y venta de los dispositivos, dado que es la institución encargada de aprobar la emisión de los Registros Sanitarios.
Los lineamientos para la importación y venta de pruebas rápidas de autodetección de covid-19 son:
- Se autorizan pruebas rápidas de detección de antígenos cuyo protocolo de toma de muestras sea exclusivamente para muestras nasales.
- Deben tener una sensibilidad mayor al 90% y una especificidad mayor al 95%.
- Deben ser de venta libre.
- Deben contener en la etiqueta el apartado para la inclusión del código QR para vigilancia epidemiológica.
Indica además el comunicado que para las personas particulares o jurídicas que estén interesadas en fabricar o importar estos dispositivos médicos en el país, los requisitos para la obtención del Registro Sanitario se encuentran establecidos en la resolución respectiva.
El ministro de Salud Pública, José Ruales, durante la reunión del Comité de Operaciones de Emergencia (COE) nacional, informó el martes 9 de agosto pasado que tras la evaluación de la situación epidemiológica del coronavirus en el país se aprobó el protocolo para la liberación de la venta de pruebas rápidas para el autodiagnóstico de covid. (I)
#ComunicadoArcsa | Lineamientos para la importación y comercialización de pruebas rápidas de autodetección #COVID_19 en el #Ecuador. #SomosArcsa ✅ pic.twitter.com/AyefWRfEjm
— Arcsa Ecuador (@Arcsa_Ec) August 12, 2022

-
Mundialísimo hace 4 días
Leonardo Campana, lesionado, baja con la selección de Ecuador para el Mundial
-
Mundialísimo hace 3 días
Cristiano encabeza la convocatoria de Portugal para el que será su último Mundial
-
Mundialísimo hace 2 días
Estados Unidos, con fiebre del Mundial FIFA 2026: Conoce qué tendrá cada ciudad con estadios sedes
-
Entretenimiento hace 4 días
Shakira sigue facturando: sentencia a favor de la cantante hará que le devuelvan millones de euros



























